Blutgefäße im Skelettsystem steuern die Knochenbildung
Forschungsbericht (importiert) 2014 - Max-Planck-Institut für molekulare Biomedizin
Knochenbildung und Blutgefäßwachstum
Wirbeltiere besitzen ein Skelettsystem aus Knochen, das auch nach dem Abschluss von Entwicklung und Wachstum noch überraschend dynamisch bleibt. Knochensubstanz wird nicht nur bei der Reparatur von Frakturen neu gebildet, sondern befindet sich während des gesamten Lebens in einem homöostatischen Gleichgewicht: Kontinuierlich werden reife Knochenzellen (Osteozyten) und deren Vorläufer (Osteoblasten) gebildet, wodurch der gleichzeitig erfolgende Abbau von Knochensubstanz durch Osteoclasten ausgeglichen wird. Im älteren Organismus oder auch bei Erkrankungen des Menschen, wie beispielsweise der Osteoporose, ist dieses Gleichgewicht gestört. Das führt zu einer zunehmenden Schwächung der Knochen und erhöht somit die Gefahr von Frakturen. Gängige Behandlungsansätze zielen in solchen Fällen auf die Steigerung der Knochenneubildung (Osteogenese) bzw. die Hemmung des Knochenabbaus. Da bestehende Therapien jedoch nicht ausreichend erfolgreich sind, ist ein besseres Verständnis der zellulären und molekularen Prozesse im Knochen dringend erforderlich.
Frühere Arbeiten hatten bereits angedeutet, dass Blutgefäße, die das Skelettsystem mit einem dichten Netzwerk durchziehen, eine wichtige Rolle bei der Osteogenese spielen könnten. Bei der Heilung von Frakturen erfolgen Blutgefäßwachstum und Knochenbildung gleichzeitig, wobei die Vorläuferzellen von Osteoblasten bestehende Bruchstellen zusammen mit den einwachsenden Gefäßen besiedeln. Defekte der Blutgefäße stehen auch mit bestimmten Erkrankungen in Verbindung, wie zum Beispiel bei der avaskulären Knochennekrose, bei der mangelnde Blutversorgung zum lokalen Absterben von Knochengewebe führt. Die physikalischen Eigenschaften von Knochen, insbesondere deren hoher Matrixanteil und Kalkeinlagerung, hatten jedoch bisher Untersuchungen mit hochauflösenden bildgebenden Verfahren und damit Einblicke in die genaue Funktion des Gefäßnetzwerks erschwert.
Neue Einblicke in die Organisation von Blutgefäßen im Knochen
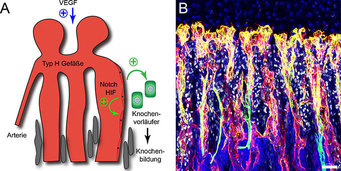
(B) Konfokalmikroskopische Aufnahme eines Gewebeschnitts aus dem Schienbein der Maus nach Färbung mit spezifischen Antikörpern. Typ-H-Gefäße erscheinen gelb aufgrund der Überlappung ihrer Markerproteine CD31 (grüne Fluoreszenz) und Endomucin (rot). Die Zellkerne von Knochenvorläuferzellen wurden durch den Nachweis des Transkriptionsfaktors Osterix (weiß) sichtbar gemacht.
Das internationale Forscherteam um Ralf Adams konnte jetzt die Methodik für die Aufbereitung, Färbung und hochauflösende Bildgebung von Knochen am Modellsystem der Maus deutlich verbessern, wodurch die Wissenschaftler eine ganze Reihe neuer Erkenntnisse gewonnen haben. So haben sie gezeigt, dass es zwei unterschiedliche Arten von Kapillaren im Knochen gibt. Typ-H-Gefäße, so benannt wegen der hohen (’high’) Expression der spezifischen Markerproteine CD31 und Endomucin, sind eng mit Knochenvorläuferzellen assoziiert und finden sich dort, wo Knochen gebildet wird. Typ-L (’low’)-Kapillaren, die den Großteil der Gefäße im Knochen ausmachen, bilden das Gefäßnetz des Knochenmarks und sind überwiegend von blutbildenden Zellen des hämatopoetischen Systems umgeben. Grund für diese Unterschiede sind die Eigenschaften der jeweiligen Endothelzellen, welche die röhrenförmigen Blutgefäße bilden. So produzieren vor allem die Zellen der Typ-H-Gefäße Wachstumsfaktoren und Signalmoleküle, die auf Knochenvorläuferzellen wirken und deren Wachstum stimulieren.
Beide Gefäßtypen sind jedoch miteinander verbunden und auch ansonsten eng miteinander verwandt. Nach Abschluss von Entwicklung und Wachstum, wandeln sich Typ-H-Gefäße kontinuierlich in den L-Typ um, so dass im alternden Knochen fast ausschließlich Kapillaren vom L-Typ existieren. Im Alter nimmt auch die Zahl der Knochenvorläuferzellen deutlich ab. Gleichzeitig verschlechtern sich, wie es auch bei alternden Menschen der Fall ist, Knochendichte und -stabilität. Daher ergab sich die Frage, ob die Erzeugung von neuen Typ-H-Gefäßen der altersbedingten Knochendegeneration entgegenwirken könnte.
Blutgefäße können die Knochenbildung im Alter erhöhen
Mit Hilfe von genetischen Verfahren in der Maus konnten die Forscher um Ralf Adams zwei Methoden identifizieren, um die Bildung von Typ-H-Blutgefäßen zu kontrollieren. Ein Abschalten der HIF- (’hypoxia inducible factor’) und Notch-Signalwege in Endothelzellen führte jeweils zu einer starken Abnahme von Typ-H-Gefäßen, dem Verlust von Knochenvorläuferzellen und zu Knochendefekten. Umgekehrt bewirkte eine Überaktivierung dieser Signale eine starke Zunahme der Typ-H-Gefäße, was auch die Zahl der Knochenvorläuferzellen erhöhte und die Knochenbildung verstärkte. Dies funktionierte so auch im gealterten Tier, wobei die Dichte und Qualität der Knochen durch eine Reaktivierung von Typ-H-Blutgefäßen deutlich verbessert wurde [1; 2].
Ausblick
Die neuen Erkenntnisse beweisen, dass Blutgefäße nicht nur für die Versorgung des Knochengewebes essenziell sind, sondern auch die Knochenbildung direkt durch die Sekretion löslicher Faktoren steuern können. Damit stellt sich jetzt die Frage, ob dies auch im menschlichen Skelettsystem so funktioniert und damit möglicherweise auch in der Zukunft therapeutisch eingesetzt werden könnte. Gleichzeitig wird erforscht, wie das Gefäßsystem des Knochens bei verschiedenen Krankheitszuständen oder auch bei regenerativen Prozessen verändert ist.
Literaturhinweise
DOI: 10.1038/nature13145
Nature 507, 376-380 (2014)
DOI: 10.1038/nature13146