Molekulare Mechanismen bei Entzündungsreaktionen
Forschungsbericht (importiert) 2012 - Max-Planck-Institut für molekulare Biomedizin
Einleitung
Neutrophile Granulozyten sind eine Untergruppe der Leukozyten und gehören zum angeborenen Immunsystem. Sie werden im Knochenmark produziert und zirkulieren für einige Stunden im Blut, bevor sie dann spezifisch in entzündetes Gewebe auswandern, das durch eine Infektion, ein Trauma oder eine Autoimmunreaktion induziert werden kann. Dieses Auswandern der Leukozyten vom Blut in entzündetes Gewebe wird als Rekrutierung bezeichnet. Neutrophile Granulozyten sind wichtig bei der Bekämpfung von bakteriell-induzierten Infektionen. Wiederkehrende bakterielle Infektionen können durch eine Störung der Rekrutierung von Leukozyten in entzündetes Gewebe verursacht werden. Im Gegensatz hierzu kann die Hemmung der Rekrutierung von Leukozyten im Rahmen entzündlicher Prozesse auch protektive Effekte haben.
Im Bereich entzündlicher Prozesse kommen neutrophile Granulozyten mit dem Endothel der Gefäßwand in Kontakt und sammeln dabei verschiedene Signale, die die Adhäsion und Transmigration, also Auswanderung vom Blut in das Gewebe, induzieren [1]. Dieser erste Kontakt zwischen neutrophilen Granulozyten und dem Endothel ist als Capturing bekannt und wird durch Selektine und deren Rezeptoren vermittelt [2]. Die Selektin-Familie besteht aus drei Glykoproteinen, die ein unterschiedliches Expressionsmuster aufweisen. L-Selektin wird konstitutiv auf der Oberfläche der meisten Leukozyten exprimiert und ist an der Rekrutierung von Leukozyten in entzündetes Gewebe beteiligt. P-Selektin wird auf aktivierten Thrombozyten und Endothelzellen exprimiert, vermittelt den primären Kontakt zwischen Endothel und Leukozyten und ist beteiligt am Rollen von Leukozyten entlang dem Endothel. E-Selektin wird auf entzündeten Endothelzellen exprimiert und ist ein Ligand für P-Selektin-Glykoprotein-Ligand (PSGL)-1 und andere Rezeptoren. Zusätzlich zum Capturing vermittelt E-Selektin Integrin-abhängiges langsames Rollen sowohl in vivo als auch in vitro und ist an der Rekrutierung von neutrophilen Granulozyten beteiligt [3].
Während die neutrophilen Granulozyten am Endothelium entlangrollen, sind sie verschiedenen entzündlichen Mediatoren ausgesetzt, die unterschiedliche Signalwege aktivieren können [4]. Diese Signalwege führen zur Aktivierung von Integrinen, die für die Migration der Leukozyten aus der Blutbahn in entzündetes Gewebe (auch Leukozyten-Extravasation genannt) notwendig sind. Die Integrine können sowohl durch G-Protein-gekoppelte Rezeptoren als auch durch die Bindung von Selektinen an ihre Rezeptoren auf neutrophilen Granulozyten aktiviert werden.
Integrine sind Adhäsionsmoleküle, die auf Leukozyten, Thrombozyten und verschiedenen anderen Zellen vorkommen [5]. Sie sind in der Zellmembran verankert und durchqueren diese. Integrine verbinden Zellen mit der extrazellulären Matrix sowie mit anderen Zellen. Weiterhin sind sie für die Signalweiterleitung zwischen Zellen und deren Umgebung bedeutsam. Diese Moleküle spielen eine wichtige Rolle bei vielen Prozessen innerhalb des Körpers. Sie sind beteiligt an der gerichteten Wanderung von Leukozyten in entzündetes Gewebe und an bestimmten Schritten der Blutgerinnung [5].
Die Forschergruppe von Alexander Zarbock untersucht die Chemokin-induzierte Anheftung von neutrophilen Granulozyten am Endothel sowie die molekularen Mechanismen des Selektin-vermittelten langsamen Rollens von neutrophilen Granulozyten. Neben neuen Mikroskopie-Techniken und verschiedenen klinisch relevanten Tiermodellen benutzt die Arbeitsgruppe auch einen translationalen Forschungsansatz, um Grundlagenforschung mit klinischer Forschung zu kombinieren.
Integrin-Aktivierung und Leukozyten-Rekrutierung: Schlüssel für eine Therapie von Störungen der Entzündungsreaktionen
Während der Interaktion von neutrophilen Granulozyten mit der Gefäßwand sind die Zellen verschiedenen Molekülen ausgesetzt, die verschiedene Signaltransduktionswege in neutrophilen Granulozyten aktivieren können. Diese Signaltransduktionswege führen zu der Aktivierung von Integrinen. Dies sind Adhäsionsmoleküle, die nach ihrer Aktivierung an Gegenrezeptoren, die auf der Gefäßwand exprimiert werden, binden können und somit bei der Auswanderung von neutrophilen Granulozyten in entzündliches Gewebe erforderlich sind. Ist diese Aktivierung von Integrinen gestört, führt das zu immer wiederkehrenden Infektionen mit der Folge, dass die Patienten mit solch einem Defekt eine verkürzte Lebenserwartung haben. Dies unterstreicht, wie wichtig der Aktivierbarkeit der Moleküle ist. Zarbock und sein Team untersuchen die intrazellulären Signalwege, die zur Aktivierung und Deaktivierung der Integrine führen.
E-Selektin vermittelt die Aktivierung von Integrin und die Rekrutierung von Leukozyten
Mit Hilfe von intravitalmikroskopischen Untersuchungen und Flusskammerexperimenten konnten die Wissenschaftler zeigen, dass die Bindung von E-Selektin an PSGL-1 das Integrin LFA-1 aktiviert [3]. Des Weiteren konnten sie zeigen, dass verschiedene Signaltransduktionsmoleküle an der Aktivierung von Integrinen nach Bindung von Selektinen an neutrophile Granulozyten beteiligt sind [6].
In einer erst kürzlich publizierten Studie konnten die Forscher den Selektin-vermittelten Signaltransduktionsweg unterhalb von Syk identifizieren. Die Bindung von E-Selektin an neutrophile Granulozyten führt zu einer Syk-abhängigen Aktivierung des Signaltransduktionsmoleküls Btk [7]. Mit Hilfe von Btk-defizienten Mäusen und verschiedenen intravitalmikroskopischen Techniken konnten die einzelnen Schritte der Rekrutierungskaskade von Leukozyten, einschließlich Capturing, Rollen, Adhäsion und Transmigration, untersucht werden.
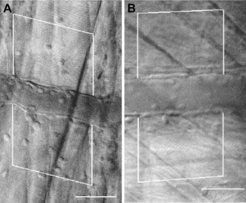
In Mäusen, welche das Signaltransduktionsmolekül Btk nicht exprimieren, war das E-Selektin-vermittelte langsame Rollen komplett aufgehoben und der Verlust von Btk führte ebenfalls zu einer verminderten Adhäsion von Leukozyten in Abwesenheit des Gαi-vermittelten Signaltransduktionsweges. Die Eliminierung von Btk in hämatopoetischen Zellen führte auch dazu, dass extravasierte Leukozyten im entzündeten Gewebe im Vergleich zu Wildtyp-Mäusen signifikant reduziert waren (Abb. 1).
Das Team um Zarbock entwickelte ein neues Flusskammersystem, welches die Untersuchung der Rollgeschwindigkeit von humanen neutrophilen Granulozyten im Vollblut ermöglicht. Mit Hilfe dieses Systems konnten sie zeigen, dass es auch nach Bindung von Selektinen an humane neutrophile Granulozyten zu einer Aktivierung von Integrinen kommt [8]. Ähnlich wie bei murinen neutrophilen Granulozyten war die Reduktion der Rollgeschwindigkeit abhängig von der Anwesenheit von PSGL-1, LFA-1, der Src-Kinase Fgr und Syk [8].
Die Arbeitsgruppe konnte zeigen, dass Mäuse, die die Signaltransduktionsmoleküle SLP-76 oder ADAP nicht besitzen, vor einem akuten Nierenversagen geschützt sind [9]. Mit Hilfe von intravitalmikroskopischen und biochemischen Methoden wurde deutlich, dass SLP76 unterhalb von Syk lokalisiert und notwendig für die Aktivierung von Btk ist. Mit Hilfe der Intravitalmikroskopie der renalen Mikrozirkulation konnte gezeigt werden, dass E-Selektin-vermitteltes langsames Rollen in der renalen Mikrozirkulation nach Ischämie-Reperfusions-Schaden vorkommt [9]. Diese Daten beweisen, dass der E-Selektin-vermittelte Signaltransduktionsweg im Rahmen dieses Krankheitsmodells einen wichtigen Signaltransduktionsweg darstellt.
Die Chemokin-vermittelte Integrin-Aktivierung und Leukozyten-Rekrutierung
Der Wachstumsfaktor Growth-Differentiation-Faktor (GDF)-15 ist ein Zytokin aus der Transforming-Growth-Factor (TGF)-β-Superfamilie, die sich aus einer großen Anzahl zum Teil sehr divergenter Zytokine mit vielfältigen Funktionen im Bereich von Gewebeentwicklung, -differenzierung und –homöostase zusammensetzt. Unter physiologischen Bedingungen ist GDF-15 in den meisten Geweben nur schwach exprimiert. Im Rahmen einer akuten Entzündungsreaktion oder als Antwort auf andere exogene Stressoren steigt die Expression von GDF-15 im betroffenen Gewebe an.
Klinische Untersuchungen legen einen potenziellen Zusammenhang zwischen GDF-15 und einem entzündlichen Geschehen nahe. Der Mechanismus, über den GDF-15 seine anti-inflammatorischen Eigenschaften vermittelt, ist bis heute nicht bekannt.
Um die anti-inflammatorischen Effekte von GDF-15 zu untersuchen, wählten die Wissenschaftler ein Tiermodell des Herzinfarkts, da in diesem Modell die Regulation der Leukozyten-Rekrutierung von entscheidender Bedeutung für die Wundheilung und Vermeidung fataler Komplikationen ist. Die Expression von GDF-15 steigt bei einem Infarkt im Herzmuskelgewebe von Mensch und Maus an [10]. Die Studie zeigte, dass der Verschluss einer Koronararterie in GDF-15-defizienten Mäusen eine gesteigerte Rekrutierung von neutrophilen Granulozyten in das Herzmuskelgewebe und mehr Komplikationen wie Risse des Herzmuskels bewirken [10]. In Rekonstitutionsexperimenten führte die kontinuierliche Applikation von rekombinantem GDF-15 in GDF-15-defizienten Mäusen zu einer verminderten Rekrutierung von neutrophilen Granulozyten in infarziertes Gewebe [10].
Diese Daten weisen darauf hin, dass GDF-15 die Rekrutierung von neutrophilen Granulozyten in entzündetes Gewebe vermindert. In-vitro-Experimente wurden durchgeführt, um zu untersuchen, ob GDF-15 direkt auf neutrophile Granulozyten wirkt und wie GDF-15 seine anti-inflammatorischen Eigenschaften vermittelt. Sie zeigten, dass rekombinantes GDF-15 die Adhäsion und Transmigration von neutrophilen Granulozyten direkt inhibiert [10]. Mit Hilfe biochemischer Experimente und Reporter-Antikörpern konnte ebenfalls nachgewiesen werden, dass GDF-15 die Chemokin-induzierte Erhöhung der Integrin-Affinität und -Avidität von β2-Integrinen auf neutrophilen Granulozyten inhibiert [10]. Diese Studie identifiziert GDF-15 als das erste Zytokin, das die Rekrutierung von neutrophilen Granulozyten durch eine Aufhebung der Chemokin-induzierten Aktivierung von β2-Integrinen inhibiert [10]. Der Verlust dieses neuen anti-inflammatorischen Mechanismus führt zu einer erhöhten Inzidenz an fatalen Herzmuskelrissen nach Herzinfarkt.
