Frischer Wind für alte Stammzellnischen
Forscher des Max-Planck-Instituts und der Universität Münster haben herausgefunden, wie sie blutbildende Stammzellen vermehren können
Blutgefäße spielen eine entscheidende Rolle beim Wachstum von Knochengewebe sowie bei der Blutbildung, der Hämatopoese. Die Blutgefäße versorgen dabei nicht nur das Knochenmark mit Sauerstoff und Nährstoffen, sondern bilden auch sogenannte vaskuläre Nischen. Die sorgen mit bestimmten Signalen dafür, dass die blutbildenden Stammzellen erhalten bleiben. Vergrößert sich die Zahl der Nischen, steigt auch die Zahl der Stammzellen an. Im alternden Organismus verschlechtert sich die Qualität der Stammzellen. Bisher war aber nicht bekannt, wie sich dabei die Nischen verändern. Forscher des Max-Planck-Instituts für molekulare Biomedizin sowie der Medizinischen Fakultät und des Exzellenzclusters „Cells in Motion“ der Universität Münster haben nun herausgefunden, wie sie die Funktion der vaskulären Stammzellnischen im Knochenmark verbessern und damit die Zahl der Stammzellen erhöhen können. Dazu manipulierten sie die Endothelzellen, also die Zellen, die Blutgefäße innen auskleiden. Diese Erkenntnisse könnten später dazu führen, Erkrankungen des Knochenmarks besser zu behandeln oder Stammzelltransplantationen individueller durchzuführen. Erschienen ist die Studie in der anerkannten Fachzeitschrift Nature (Advance Online Publication 13. April 2016).
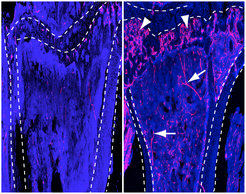
Die Funktion der Stammzellen im Knochenmark nimmt mit zunehmendem Alter ab. Das ist darauf zurückzuführen, dass die Zellen altern und sich die Funktion der vaskulären Nischen verschlechtert. Die Wissenschaftler um Dr. Anjali P. Kusumbe und Prof. Ralf H. Adams untersuchten diese Vorgänge in Mäusen. Sie sahen sich das alte Knochenmark genauer an und entdeckten dabei, dass sich das Gefäßnetzwerk im alternden Knochen grundlegend verändert. So nimmt die Zahl der Arterien und bestimmter Kapillaren deutlich ab. Außerdem gibt es weniger Bindegewebszellen um die Blutgefäße, sogenannte mesenchymale Zellen. Die Produktion von Signalen für blutbildende Stammzellen verringert sich ebenfalls.
Gleichzeitig fanden die Forscher heraus, wie sie vaskuläre Nischen und damit die Zahl der blutbildenden Stammzellen vermehren können. Hierzu aktivierten sie Endothelzellen in der innersten Schicht der Blutgefäßwand. Dies erfolgte über den sogenannten Notch-Signalweg, mit dem benachbarte Endothelzellen miteinander kommunizieren und ihr Verhalten abstimmen. Bei der Aktivierung des Notch-Signalwegs kommt es zur Vermehrung von speziellen Kapillaren, zur Bildung kleiner Arterien und zur Zunahme der mesenchymalen Bindegewebszellen um die Blutgefäße. Gleichzeitig steigt die Produktion von Signalen für die blutbildenden Stammzellen im Knochenmark. „Nur all diese Faktoren zusammen erzeugen neue Stammzellnischen, wogegen ohne neue Arterien und mesenchymale Zellen keine vaskulären Nischen gebildet werden“, sagt Ralf Adams. Damit entschlüsselten er und seine Forscherkollegen ein hochkomplexes System.
Auch im Endothel alter Mäuse konnten die Wissenschaftler die Zahl der vaskulären Stammzellnischen vergrößern, indem sie den Notch-Signalweg aktivierten und so das Endothel manipulierten. Den Alterungsprozess der blutbildenden Stammzellen konnten sie dabei allerdings nicht rückgängig machen. „Die Manipulation des Endothels und die damit verbundene Vermehrung von Stammzellnischen könnte aber für die Behandlung von Erkrankungen des Knochenmarks oder bei der therapeutischen Stammzelltransplantation von Bedeutung sein“, gibt Ralf Adams einen Ausblick für die Zukunft. Konkret beträfe das zum Beispiel ältere Menschen oder Patienten, die unzureichend auf eine Stammzelltransplantation reagieren.
Die Studie entstand aus einer internationalen Zusammenarbeit verschiedener Forschungsinstitute aus Deutschland, Israel und Schweden. Aus Münster waren das Max-Planck-Institut für molekulare Biomedizin sowie die Medizinische Fakultät und der Exzellenzcluster Cells in Motion (CiM) der Universität Münster beteiligt. Ralf Adams leitet eine der rund 80 Forschergruppen des Clusters.
CiM
