Dem Mechanismus der Arterienbildung auf der Spur
Wissenschaftlerteam aus Münster und Gießen weist Zusammenhang zwischen Notch-Signalweg und Arterienbildung nach – Neuer Mechanismus, der auch für kardiovaskuläre Erkrankungen relevant sein könnte
Arteriogenese ist ein elementares Ereignis – nicht nur während der Entwicklung, sondern auch im Erwachsenenleben. Kardiovaskuläre, lebensbedrohliche Krankheiten könnten von Alternativen zu schon bestehenden Therapien überwunden werden, zum Beispiel wenn die Bildung neuer Arterien angeregt werden könnte. Über die Mechanismen der Arterienbildung ist jedoch nicht viel bekannt. Ein Wissenschaftlerteam um Ralf Adams des Max-Planck-Instituts für molekulare Biomedizin in Münster hat einen eleganten genetischen Ansatz in Mäusen entwickelt, um die molekularen Mechanismen, die das Arterienwachstum koordinieren, aufzudecken. Zusammen mit Tilman Borggrefe und seinen Kollegen des Biochemischen Institutes der Justus-Liebig-Universität Gießen fanden sie heraus, dass ein Rezeptor namens Notch in diesem Prozess essenziell ist: hohe Notch-Aktivität bringt sprießende Zellen der vordersten Wachstumsfront dazu, sich in entwickelnde Arterien einzugliedern. Dies ist die erste Studie in Mäusen, die den Beweis für eine direkte Verbindung zwischen angiogener Sprossung und Arterienbildung liefert. Diese Erkenntnisse aus der postnatalen Entwicklung könnten dabei helfen, neue therapeutische Ansätze zu identifizieren, die die Bildung neuer Arterien nach Organverletzungen anregen (Nature Cell Biology, online vorab, 17. Juli 2017).
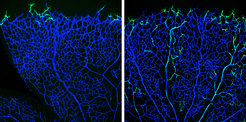
Genetisch markierte Leitzellen (grün) 12 Stunden nach Pulse-Chase (links) in einem Gefäßplexus (blau) der Retina einer 6 Tage alten Maus. Nach 96 Stunden befinden sich die meisten Leitzell-Nachkömmlinge in den Arterien, aber nicht in den Venen.
Das Blutgefäßsystem bildet ein komplexes Netzwerk von Arterien, Venen und Kapillaren und transportiert Sauerstoff, Nährstoffe, Zellen und Abfallprodukte durch unseren Körper. Demzufolge spielt die Vaskulatur eine sehr wichtige Rolle in nahezu allen Körperfunktionen.
Kardiovaskuläre Störungen, wie zum Beispiel Herzinfarkt oder Schlaganfälle, werden durch funktionsgestörte Arterien verursacht und sind mittlerweile weltweit die häufigste Haupttodesursache. Erkenntnisse über die Bildung und das Wachstum von Arterien unter physiologischen Bedingungen könnten für die Identifikation neuer therapeutischer Ansätze zur Wachstumsstimulierung neuer Arterien unter pathologischen Bedingungen ungemein wichtig sein. Vor allem die Arterienbildung ist wichtig, denn nur dieser Gefäßtyp kann genügend Blut in die beeinträchtigten Gewebe transportieren. Wie das vaskuläre Netzwerk aufgebaut ist, ist noch nicht ausreichend gut erforscht – noch weniger ist bekannt, wie die Arteriogenese in therapeutischen Ansätzen stimuliert werden könnte.
Max Planck Wissenschaftler des Labors von Ralf Adams haben nun die Angiogenese – die Bildung neuer Blutgefäße aus einem bestehenden Kapillarnetzwerk – im Gefäßnetzwerk der Retina von neugeborenen Mäusen untersucht.
„Die so genannten Leitzellen tasten im wachsenden Gefäßnetzwerk ihre Umgebung ab und weisen den nachfolgenden Endothelzellen die richtige Richtung“, sagt Mara Pitulescu, Erstautorin der Studie und Wissenschaftlerin in der Abteilung von Ralf Adams. Leitzellen werden gefolgt von so genannten Stalk-Zellen (to stalk, engl.: verfolgen), welche einen proliferativeren Charakter haben. Direkt hinter den Leit- und Stalk-Zellen sind die Blutgefäße zunächst in einem unausgereiften Plexus arrangiert, von dem aus Arterien, Venen und die verbindenden Kapillaren gebildet werden. Mittels Signalmoleküle interagieren Endothelzellen in diesem Netzwerk andauernd mit benachbarten Zellen und ihrer Umgebung. Diese Interaktionen basieren auf Rezeptoren, die sich auf der Oberfläche von Endothelzellen befinden und auf Liganden, die an die Rezeptoren binden. Vor allem der Notch-Rezeptor und sein Ligand Dll4 sind, neben anderen Rezeptoren und Liganden, für die Angiogenese wichtig.
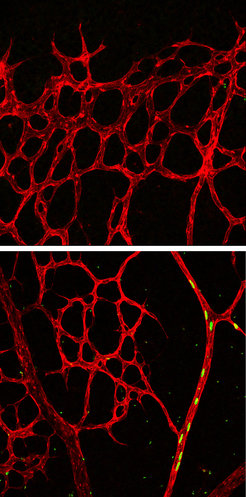
Überexprimierung von aktivem Notch bringt alle markierte Abkömmlinge (grün, Zellkerne) in die Arterien des vaskulären Plexus der Retina (rot; Bild unten; 96 Stunden nach Pulse-Chase-Experiment). In der Expansionszone des peripheren Plexus sind keine markierten Zellen mehr vorhanden (Bild oben).
Pitulescu kombinierte genetische Experimente mit pharmakologischen Methoden. „Dieser Ansatz ermöglichte es uns, zwischen Signalen für Zell-Zell-Interaktionen und der Signalkaskade rein innerhalb der Endothelzellen zu unterscheiden“, erklärt Pitulescu. „Wir beobachteten, dass die Notch-Aktivierung an sich wichtiger ist als die eigentliche Notch-basierte Zell-Zell-Kommunikation. Dies ist eine neue Erkenntnis“, sagt Pitulescu.
Lange Zeit wurde zur Expansion eines Gefäßnetzwerkes gedacht, dass die unterversorgte Umgebung Signale abgibt, denen die Leit- und Stalk-Zellen folgen, während das Gefäßnetzwerkes hinter diesen Zellen in die unterversorgte Richtung mitwächst. Mit dem vaskulären Plexus erweitern sich auch die Arterien. In einer früheren Studie von Arndt Siekmann des MPIs für molekulare Biomedizin konnte er in Zebrafischen zeigen, dass Arterien hauptsächlich gebildet werden durch Endothelzellen, die aus Venen sprießen und sich dann entgegen der allgemeinen Wachstumsrichtung bewegen.
Um die genauen Mechanismen der Arterienbildung in Mäusen zu studieren, verwendete das Team um Ralf Adams einen eleganten genetischen Ansatz in Mäusen, bei dem nur die Leitzellen und deren Abkömmlinge markiert werden und über die Zeit verfolgt werden können. „Erstaunlicherweise fanden wir heraus, dass die Abkömmlinge der Leitzellen entgegen der allgemeinen Wachstumsrichtung des Plexus migrieren und sich innerhalb einiger Tage in Arterien integrieren“, sagt Pitulescu.
Die Wissenschaftler konnten den Notch-Ligand Dll4 in Leitzellen gezielt inaktivieren und beobachten, wie sich das Gefäßnetzwerk ausbreitete. Interessanterweise ist Dll4 nicht erforderlich, um Leitzellen in ihrer Position am Rande des wachsenden Gefäßbettes zu halten. „Vielmehr fanden wir heraus, dass CXCR4, ein für Zellmigration wichtiger Chemokin-Rezeptor, für die Erhaltung der Leitzellen notwendig ist“, sagt Pitulescu. Die Experimente verdeutlichten allerdings die Rolle von Dll4: „Wenn Dll4 nicht vorhanden ist und der Notch-Rezeptor dadurch nicht aktiviert wird, verschlechtert sich die Rückwärts-Migration der Leitzellen“, sagt Pitulescu.
„Dies ist die erste Studie in Mäusen, in der gezeigt wird, dass die direkte Verbindung zwischen Sprossung und Arterienbildung gleichermaßen von Notch reguliert wird“, sagt Ralf Adams, der auch Professor der Medizinischen Fakultät der Westfälischen Wilhelms-Universität Münster und Mitglied des Exzellenzclusters „Cells in Motion“ ist.
„Diese Ergebnisse sind von großer Bedeutung für das Verständnis des arteriellen Wachstums“, sagt Tilman Borggrefe, der mit seinem Team die biochemischen Analysen der Studie durchführte. „Dies könnte die Grundlage für einen neuen therapeutischen Ansatz sein, in dem bei Bedarf an Arterienbildung die Angiogenese über Notch kontrolliert werden könnte“, sagt Borggrefe.

