3D-Genomorganisation unabhängig von der Genregulation in Drosophila
Wie kann man zwei Meter DNA in den Kern einer Zelle packen und sicherstellen, dass die richtigen Gene in der richtigen Zelle zur richtigen Zeit exprimiert werden?
Zu verstehen, wie unsere Gene funktionieren können, wenn die gesamte genetische Information in den Zellkern verpackt ist, ist für die Forscherinnen und Forscher des Max-Planck-Instituts für molekulare Biomedizin in Münster und der Gruppe Developmental and Regulatory Genomics am MRC London Institute of Medical Sciences (LMS) eine Schlüsselfrage ihrer Arbeiten. Unser fundamentales Verständnis für die Rolle der 3D-Organisation des Genoms und der Regulation der Genexpression zu erweitern kann uns dabei helfen, Veränderungen, die zu Mutationen und Krankheiten wie Krebs führen, besser zu verstehen.
Frühere Studien haben gezeigt, dass die Genomorganisation eng mit der Genexpression und der Genregulation verbunden ist. Jüngste Forschungen des Forscherteams zeigten, dass die 3D-Genomstruktur des Drosophila-Embryos zu Beginn der zygotischen Genomaktivierung etabliert wird. Das ist das frühe Embryonalstadium, in dem die Expression der meisten Gene beginnt und der Embryo anfängt Zellen zu bilden. Dieses Stadium des Drosophila-Embryos entspricht ungefähr dem 4-Zell-Stadium des menschlichen Embryos und dem 2-Zell-Stadium des Mausembryos. Wie die 3D-Genomorganisation dann jedoch während der Differenzierung von Zellen später in der Embryonalentwicklung reguliert wird, ist unbekannt.
Mit Drosophila-Embryonen in diesem Entwicklungsstadium als Modellsystem untersuchten die Forscher den Zusammenhang zwischen 3D-Genomorganisation, Genexpression und Genregulation. Konkret wollten sie wissen, wie heterogen die Chromatinkonformation im gesamten Embryo ist und ob Entwicklungstranskriptionsfaktoren oder Genregulation die Genomorganisation beeinflussen. „Schon in diesem frühen Entwicklungsstadium weist der Embryo ein komplexes Muster von Morphogen-Gradienten auf, die letztendlich entscheiden, welche Zellen bestimmte Gewebe bilden“, sagt Liz Ing-Simmons, Erstautorin der Arbeit.
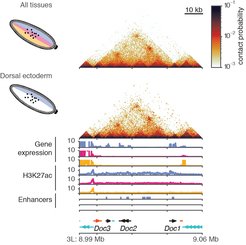
Der Drosophila-Embryo hat eine anterior-posteriore Achse und eine dorsal-ventrale Achse. In dieser Studie nutzten die Forscher die dorsal-ventrale Musterung, um zu untersuchen, wie heterogen die Chromatinkonformation im gesamten Embryo ist. Die Spezifikation der Gewebe im Embryo wird durch die Konzentration des Transkriptionsfaktors Dorsal (DI) in den Zellkernen bestimmt. Die Konzentration des Dorsal-Proteins im ventralen Teil des Embryos ist höher, was zu Mesoderm-Entwicklung führt. Im dorsalen Teil ist die Konzentration niedriger, was zu dorsalem Ektoderm führt, während eine mittlere Konzentration dazu führt, dass sich Neuroektoderm entwickelt.
Die Forscher verwendeten drei Modelle mit Mutationen in dem Signalweg, der die Konzentration des Transkriptionsfaktors Dorsal steuert (hoch, mittel, niedrig), die von Mitarbeitern der Universität Stockholm, Schweden, zur Verfügung gestellt wurden. Im Prinzip erwartete das Forscherteam, dass die Mutationen zu Embryonen mit einheitlichem Gewebetyp führen würden: komplett dorsales Ektoderm, komplett Neuroektoderm oder komplett Mesoderm. Dieser Ansatz ermöglichte es den Forschern zu sehen, ob es in der Chromatinkonformation in diesen drei Geweben Unterschiede gibt.
Zunächst bestätigten die Forscherinnen und Forscher, dass die drei Mutantenmodelle unterschiedliche Chromatinzustände aufgrund der Aktivierung verschiedener Enhancer und unterschiedlicher Genexpression aufwiesen. Ihre nächste Frage war: Haben diese drei Gewebe eine unterschiedliche 3D-Chromatinorganisation? Überraschenderweise fanden sie heraus, dass es insgesamt keine Unterschiede in der 3D-Genomorganisation von gewebespezifischen Genen in den drei untersuchten Gewebetypen gab.
Um dies genauer zu untersuchen, setzten die Forscher in Zusammenarbeit mit Wissenschaftlern der Princeton University, USA, zum ersten Mal die Micro-C-Technik in Drosophila ein. Mit dieser Technik konnten sie die Chromatinorganisation mit einer höheren Auflösung, als die Hi-C Technik ermöglicht, untersuchen und mehrere kleine Domänen aufdecken, die mit Hi-C nicht sichtbar waren. Selbst mit der erhöhten Auflösung der neuen Datensätze sah die 3D-Genomorganisation in den mutierten Fliegen jedoch identisch aus.
Juanma Vaquerizas, leitender Autor, sagte: "Der erhöhte Detailgrad, den Micro-C bietet, ist ein großer Durchbruch. Diese Technik wird es uns ermöglichen, feine Unterschiede in der Chromatinorganisation zwischen Proben zu untersuchen und zu verstehen, wie diese bei Krankheiten beeinträchtigt wird".
Insgesamt zeigen die Ergebnisse des Forscherteams, dass eine Veränderung des Chromatinzustands oder der Genexpression nicht ausreicht, um die 3D-Genomorganisation zu verändern. Diese Ergebnisse unterstreichen die Rolle des 3D-Genoms als architektonisches Gerüst für die Genregulation und eine unterschiedliche Organisation von entwicklungsregulierten und Housekeeping-Genen im Drosophila-Genom.
In Zukunft wird die Gruppe Developmental and Regulatory Genomics die Chromatinorganisation in verschiedenen Systemen mit Techniken wie Micro-C untersuchen, um weitere Erkenntnisse über die 3D-Genomorganisation zu gewinnen.
Die Studie 'Independence of chromatin conformation and gene regulation during Drosophila dorsoventral patterning' wurde am 1. April 2021 in der Zeitschrift Nature Genetics veröffentlicht. Lesen Sie den vollständigen Artikel hier. https://dx.doi.org/10.1038/s41588-021-00799-x
Engl. Text: Dr. Jenna Stevens-Smith, MRC LMS
