Tierschutzforschungspreis 2021 für Max-Planck-Forscher
Auszeichnung für die maschinelle Herstellung und Analyse von menschlichen dreidimensionalen Geweben für die Arzneimittel- und Toxizitätsforschung
Ohne Versuche an Tieren lassen sich kaum neue Erkenntnisse zur Funktionsweise unseres Gehirns gewinnen. Auch für die Testung neuer Medikamente werden Versuchstiere benötigt. Ein Verfahren, das Jan Bruder und Henrik Renner am Max-Planck-Institut für molekulare Biomedizin in Münster entwickelt haben, soll dazu beitragen, die Anzahl der dafür notwendigen Tierversuche zu verringern. Die Forscher haben aus Vorläufern menschlicher Gehirnzellen dreidimensionale Gewebekulturen gezüchtet, die sich in ihren Kulturschalen zu Stecknadelkopf-großen organähnlichen Gewebeverbänden entwickeln, sogenannten Organoiden. Die beiden Wissenschaftler im Team von Hans Schöler haben zudem ein automatisiertes Herstellungsverfahren entworfen, mit dem sie die Organoide standardisiert und in hoher Zahl produzieren und analysieren können. Die Organoide können in der Grundlagenforschung zu neurologischen Erkrankungen eingesetzt werden. Außerdem bräuchten Wirkstoffkandidaten, die sich in den Organoiden als unwirksam oder toxisch erweisen, nicht mehr in Tierversuchen untersucht zu werden. Für diese Technologie hat ihnen das Bundesministerium für Ernährung und Landwirtschaft den Tierschutzforschungspreis 2021 verliehen.

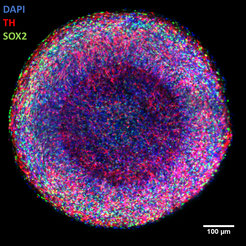
Mitte: gesamtes Organoid (rot: Marker für junge Neurone).
Rechts: Zentrum des Organoids (blau: Zellkerne; rot: junge Neurone; grün: Marker für neuronale Stammzellen)
Um die Funktionsweise des Gehirns aufklären und Medikamente gegen Erkrankungen wie Alzheimer, Parkinson oder Depression entwickeln zu können, müssen Forschende die Gehirne von Versuchstieren untersuchen. Nervenzellen lassen sich aber auch in zweidimensionalen Zellkulturen von Versuchstieren studieren. Traditionell gedeihen sie dabei in einer Nährlösung und bilden auf dem Plastikboden von Zellkulturgefäßen einen Rasen miteinander verbundener Nervenzellen. Diese flach ausgebreiteten Zellkulturen entsprechen jedoch nur entfernt den Bedingungen in einem Gehirn mit seinen unterschiedlichen Zelltypen und dreidimensionalen Netzwerken. Außerdem stammen die Nervenzellen von Tieren und lassen sich deshalb nur begrenzt mit menschlichen Gehirnzellen vergleichen.
Ganz anders die Gehirn-Organoide aus Münster. Sie entstehen aus speziellen neuralen Vorläuferzellen, die spontan selbst Gewebestückchen formen und sich in allen drei Raumrichtungen vernetzen können. Diese Zellen können die für die Organoide relevanten Zelltypen besonders schnell und zuverlässig hervorbringen. Durch ihre dreidimensionale Anordnung ahmen sie die charakteristischen Eigenschaften des natürlichen Hirngewebes besser nach als die klassischen Zellkulturen. Noch werden Organoide zum großen Teil einzeln von Hand hergestellt. Dadurch variieren sie individuell sehr stark und besitzen unterschiedliche Eigenschaften. Außerdem lassen sie sich so nicht in großen Stückzahlen produzieren. Beides ist aber notwendig, um sie für die Arzneimittelforschung einsetzen zu können.
Vollautomatische Erzeugung von Organoiden

Jan Bruder und Henrik Renner, Mitarbeiter im Forscherteam um Hans Schöler, haben ein Verfahren entwickelt, mit dem sie Organoide verschiedener Gehirnregionen tausendfach parallel züchten und für die Wirkstoffentwicklung einsetzbar machen können. Sie haben sich dabei auf das Mittelhirn konzentriert – eine Region, in der unter anderem bei Parkinson viele Nervenzellen absterben. In einem vollautomatischen Verfahren erzeugen die Wissenschaftler mit einem Pipettierroboter beliebig viele Organoide und lassen sie sich bis zur gewünschten zellulären Reife entwickeln. Dank der exakten Standardisierung der Arbeitsschritte und hohen Gleichheit der erzeugten Proben können sie die Auswirkungen von Krankheiten und möglichen Wirkstoffkandidaten oder Toxinen auf die Gewebe genau analysieren.
Analysen der Forscher zeigen, dass die automatisiert produzierten Mittelhirn-Organoide dem menschlichen Mittelhirn mindestens genauso ähnlich sind wie die von Hand hergestellten Organoide. „Sie beinhalten viele der von Parkinson zuerst geschädigten Dopamin-produzierenden Nervenzellen. Diese sind elektrisch aktiv und erzeugen komplexe, spontane auftretende und zum Teil synchrone Aktivitätsmuster“, erklärt Henrik Renner.
Auswirkungen von Krankheiten und Giftstoffen
Durch die hohe Reproduzierbarkeit der Organoide können die Forscher darüber hinaus selbst feinste Auswirkungen von Krankheiten oder Toxinen in Organoiden automatisiert untersuchen. „Wir können mit unseren Mittelhirn-Organoiden das Absterben von dopaminergen Nervenzellen in einem aktiven, menschlichen Gehirn-ähnlichem Gewebe beobachten – dieselben Zellen, die auch bei Parkinson bevorzugt Schaden nehmen. Sie haben großes Potenzial, die nächste Generation eines neuartigen Krankheitsmodells für diese Erkrankung zu werden. Außerdem können wir die Auswirkung von Giften wie zum Beispiel Pestiziden auf die Organoide vollautomatisch bestimmen“, sagt Jan Bruder.
Die Forscher haben ihre Technologie für einen Einsatz in der pharmazeutischen Industrie konzipiert. „Ich gehe davon aus, dass unser System mittelfristig wenigstens einen Teil der Tierversuche in der neurologischen und pharmakologischen Forschung überflüssig machen wird. Wirkstoffe, die in unserem Versuchssystem toxisch wirken oder nicht ausreichend wirksam sind, könnten frühzeitig aus der Entwicklung ausgeschlossen werden und müssten überhaupt nicht mehr in Tieren getestet werden“, so Bruder.


